Introduction
Une urétrite est une inflammation de l’urètre, la grande majorité sont des IST.
On parle d’urétrite aiguë lorsqu’on observe :
- un écoulement urétral abondant franchement purulent (jaune verdâtre),
- un prurit du canal urétral et des brûlures au moment de la miction
- une dysurie (= difficulté à vider la vessie) et/ou pollakiurie (envie d’uriner fréquente).
Tandis que lors d’urétrite subaiguë, l’écoulement urétral est cette fois peu abondant, clair, séreux se limitant souvent à une simple goutte matinale. Dans ce cas, il n’y a pas de brûlures au moment de la miction.
Un écoulement chez l’homme en dehors de la miction est toujours pathologique.
En France, le taux d’incidence annuel serait de 96 cas / 100 000 habitants.
Chlamydia trachomatis et Neisseria gonorrhoeae sont les deux principaux agents d’urétrites.
Agents responsables d’urétrites
Dans 50% des cas, l’étiologie de l’urétrite reste inconnue.
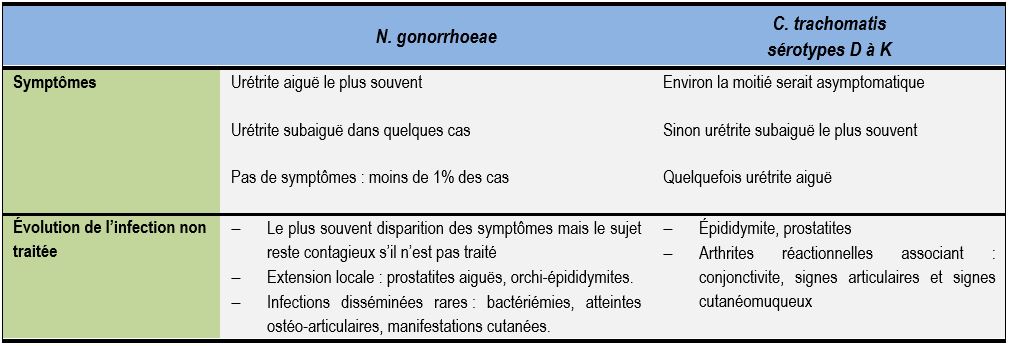
Urétrite à Chlamydia trachomatis (sérotypes D à K)
C. trachomatis est la première cause d’IST dans les pays industrialisés et la première étiologie connue d’urétrite. Ainsi en France, elle est responsable de 20 à 30% des urétrites.
Elle est asymptomatique environ une fois sur deux. Si des signes cliniques apparaissent, elle se présente alors :
- le plus souvent comme une urétrite subaiguë avec écoulement clair, séreux et peu abondant ;
- quelquefois comme une urétrite aiguë avec écoulement abondant, purulent accompagné de vives brûlures mictionnelles
L’incubation est longue (moyenne 10-15 jours).
En 2009, en Europe, l’incidence chez l’homme s’élève à 152 cas /100 000. Les personnes à risque sont jeunes (26 ans en moyenne), résident en Ile-de-France et ont eu récemment un nouveau partenaire. La tendance est à l’augmentation mais témoigne aussi d’un dépistage mieux ciblé sur les personnes à risque.
Le traitement de première intention utilise un macrolide (azythromycine) ou une cycline (doxycycline). En absence de traitement, l’infection peut se compliquer de prostatite et d’épididymite.
Urétrite gonococcique
L’urétrite gonococcique représente 10% des urétrites en France. C’est également une IST. Au contraire de ce qu’on observe chez la femme, elle est presque toujours symptomatique chez l’homme. Après une incubation silencieuse courte (2 à 7 jours), elle se manifeste dans 90% des cas par un écoulement urétral purulent, une dysurie et des brûlures mictionnelles intenses. Ainsi ces symptômes lui valent l’appellation de «chaude pisse ».
Elle s’accompagne quelquefois d’anorectite et d’oropharyngite.
L’urétrite gonococcique est en recrudescence, en France, depuis 1998 et continue de progresser en 2010 conséquence d’une augmentation des comportements sexuels à risque : défaut d’utilisation de préservatifs, partenaires multiples. Elle touche davantage les homosexuels que les hétérosexuels mais l’écart s’amenuise.
Cette infection est souvent associée à d’autres IST comme celles à C. trachomatis et chez les homosexuels masculins, à la syphilis, à l’infection à Herpes Simplex Virus 1 et 2, à l’infection au VIH et à la LGV.
En l’absence de traitement, l’infection peut se compliquer en prostatite et orchi-épididymite notamment. Les formes systémiques sont possibles mais rares : atteintes ostéo-articulaires et manifestations cutanées.
Le gonocoque a la capacité d’acquérir rapidement divers mécanismes de résistance aux antibiotiques. Ces résistances concernent la pénicilline, la tétracycline, la ciprofloxacine, et dernièrement sont apparues des souches moins sensibles aux céphalosporines de troisième génération, comme le céfixime. On administre aussitôt après le prélèvement un traitement antibiotique probabiliste antigonococcique et antichlamydia. L’AFSSAPS recommande l’association ceftriaxone – azithromycine.
Tableau 6 : Symptômes et évolution des urétrites à N. gonorrhoeae et à Chlamydia trachomatis chez l’homme
Autres agents impliqués dans les urétrites
- Mycoplasma genitalium serait la 3ème cause d’urétrite, il entraine un écoulement mucopurulent. C’est une IST
- Trichomonas vaginalis est parfois en cause : l’urétrite est le plus souvent asymptomatique ou subaiguë. C’est une IST.
- Ureaplasma spp : cette espèce, présente quelquefois à l’état commensal, est considérée pathogène si sa concentration dépasse un certain seuil.
- Candida albicans est surtout responsable de balanites (inflammation du gland) et de rares urétrites subaiguës,
- Germes pyogènes : Haemophilus spp, des streptocoques, des entérobactéries.
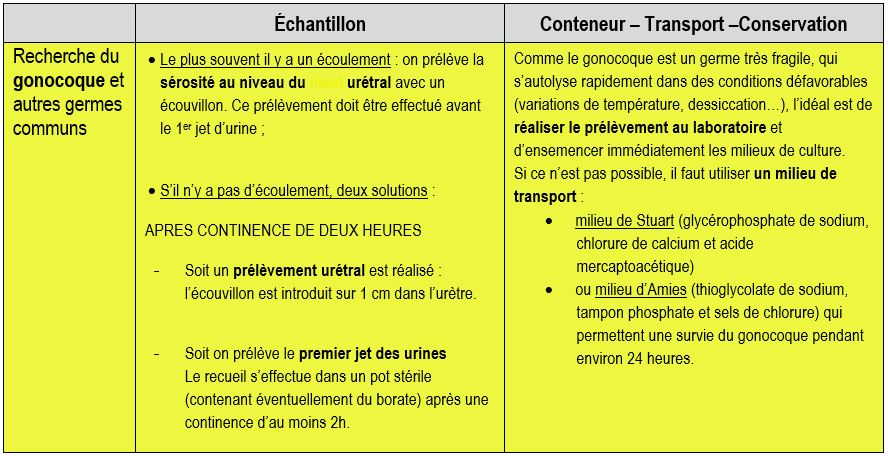
Modalités de prélèvements
| Schéma récapitulatif |
Il existe trois façons de prélever pour le diagnostic des urétrites : prélèvement de l’écoulement urétral, prélèvement urétral et 1er jet urinaire.
On recherche systématiquement à la fois les germes cultivant sur les milieux usuels (dont Neisseria gonorrhoeae) et Chlamydia trachomatis. En revanche, on recherche les mycoplasmes seulement sur prescription explicite du médecin.
On effectue ces prélèvements avant le traitement antibiotique et sans toilette ni désinfection préalable.
Pour les prélèvements urétraux et de 1er jet urinaire le patient doit se retenir d’uriner 2 heures avant le prélèvement.
| Recherche de Chlamydia trachomatis | Voir chapitre « Diagnostic des infections génitales à Chlamydia trachomatis » |
| Recherche des mycoplasmes | Voir chapitre « Diagnostic des infections génitales à mycoplasmes» |
Remarque : le comité d’infectiologie de l’Association française d’urologie (CIAFU) recommande de ne plus réaliser de prélèvement urétral à la curette (instrument métallique qui permettait de racler les muqueuses afin de recueillir des cellules.
Examens microscopiques
Les examens microscopiques permettent de poser le diagnostic d’urétrite et d’orienter quelquefois l’identification de l’agent causal.
Ils sont réalisés après la mise en culture à cause de la fragilité de certains germes (gonocoque).
On réalise alors un état frais, un frottis coloré au MGG et un frottis coloré au GRAM.
Poser le diagnostic d’une urétrite
Le diagnostic d’une urétrite repose sur une évaluation de l’intensité de la réaction inflammatoire. Une urétrite se caractérise :
- sur un frottis du prélèvement urétral ou de l’écoulement urétral coloré au MGG par la présence d’au moins 5 granulocytes par champ au grossissement × 1 000.
- sur un état frais du culot de centrifugation d’un premier jet urinaire par un nombre de granulocytes ≥ 10/champ au grossissement x 400.
Orienter l’identification de l’agent causal
État frais
En premier lieu, l’état frais est intéressant pour rechercher Trichomonas vaginalis (mobilité saccadée). Il doit être réaliser dans les 15 minutes qui suivent le prélèvement, sinon poursuivre sa recherche sur le frottis coloré au MGG.
Frottis coloré au Gram
- Son principal intérêt est d’orienter le diagnostic. Il faut noter l’abondance, sur le frottis, de chaque type de germe observé.
- Il peut permettre plus particulièrement le diagnostic présomptif d’une gonococcie aiguë par la présence de très nombreux granulocytes dont certains contiennent des diplocoques à Gram négatif en « grains de café » (Cf. fig. 32). Neisseria gonorrhoeae a, en effet, la propriété de se multiplier dans les granulocytes. Les localisations extracellulaires sont surtout le fait d’éléments libérés par la lyse des granulocytes. Lles germes sont observés alors au voisinage des débris cellulaires. L’examen microscopique est moins évocateur si l’urétrite gonococcique est subaiguë.
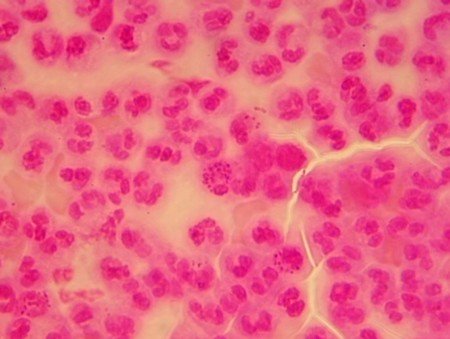
Ces examens microscopiques ne permettent pas de mettre en évidence des Chlamydiae ou des mycoplasmes. Les méthodes employées pour rechercher ces germes feront l’objet de deux autres chapitres.
Culture (Chlamydia trachomatis et mycoplasmes exclus)
Le gonocoque est une bactérie fragile et exigeante qui nécessite pour sa croissance du glucose, des facteurs de croissance (NAD, cystéine ou méthionine, bases puriques et pyrimidiques, vitamines du groupe B). Il est inhibé par les acides gras, le cholestérol, et certains métaux lourds contenus dans les géloses. Ces substances sont neutralisées par l’addition de sang ou d’amidon de maïs. Le gonocoque exige aussi un degré hygrométrique élevé et une atmosphère enrichie en CO2 (5-10 %).
On ensemence en systématique :
- un milieu riche non sélectif additionné d’un supplément vitaminique : gélose chocolat enrichie : sur un tel milieu la flore associée prolifère abondamment ;
- et un milieu riche sélectif : gélose chocolat enrichie + un mélange d’antibiotiques (VCN ou VCF ou VCAT). La vancomycine inhibe les Gram +, la colistine la plupart des Gram -, la nystatine et l’amphotéricine B (également appelé fungizone) les champignons. Le triméthoprime complète le spectre antibactérien de l’association vancomycine-colistine. Ce milieu est très sélectif du gonocoque mais 3 % des gonocoques, sensibles à la vancomycine, n’y cultivent pas.
On ensemence ces milieux sans attendre et on les incube à 35°-37C sous atmosphère humide et enrichie en CO2 pendant au moins 72 h.
On peut ajouter d’autres milieux aux précédents :
- une gélose au sang frais +/- ANC (37°C sous 5 à 10% de CO2) : elle permet de repérer les colonies de streptocoques et de staphylocoques ;
- un milieu sélectif des bacilles à Gram négatif non exigeants (Drigalski, Mac Conkey)
- un milieu sélectif pour les levures : gélose Sabouraud + chloramphénicol.
Identification, antibiogramme et interprétation des résultats (Chlamydia trachomatis et mycoplasmes exclus)
Le cas du gonocoque : identification et antibiogramme systématique
Les colonies suspectes sur géloses chocolat (non sélective et sélective) sont petites (0.5-1mm) grisâtres, à bords réguliers.
- On réalise un GRAM, les tests oxydase et catalase et on ensemence une galerie miniaturisée type Api NH® (bioMérieux) ou Neisseria 4H ® (BioRad). Le gonocoque est un diplocoque Gram – en grain de café, oxydase + et catalase +, il est glucose positif, mais maltose et saccharose négatifs.
- Un antibiogramme sur gélose chocolat enrichie est indispensable pour repérer les résistances acquises. On doit également rechercher une bêta-lactamase par un test chromogénique à la nitrocéfine (test céfinase®). Un diamètre d’inhibition plus faible autour du disque d’amoxicilline (AMX) qu’autour du disque d’amoxicilline + acide clavulanique (AMC) est aussi une preuve indirecte de la présence d’une pénicillinase. Le test « PEN » dans la galerie API NH donne de faux négatifs en raison de la faible durée d’incubation. (On peut réincuber la galerie 2h de plus en cas de réaction douteuse à ce test).
Le cas des autres germes
On identifie et on réalise un antibiogramme de tout germe présent en quantité abondante qu’il soit en culture pure ou seulement en dominance. La présence à l’examen direct d’au moins 5 granulocytes /champ (2+) et la dominance de ce même germe sont des éléments indicatifs de sa responsabilité dans l’infection.
La présence d’une culture polymicrobienne, peu abondante, laisse suspecter une simple colonisation de l’urètre par des micro-organismes de la flore cutanée, intestinale (ou vaginale chez la femme).
Diagnostic par amplification génique
Les tests basés sur l’amplification génique, indispensables pour le diagnostic des urétrites à Chlamydia trachomatis et Mycoplasma genitalium, peuvent aussi être utilisés pour le diagnostic des urétrites à gonocoque. Ils présentent de nombreux avantages :
- Ils ne requièrent pas la viabilité des bactéries
- iIls sont adaptés à tous les sites de prélèvement, y compris les premiers jets d’urines
- Les faux positifs et faux négatifs sont rares et leur performance dans le cas de patients asymptomatiques est supérieure à celle de la culture.
- La plupart sont des tests multiplex qui permettent le dépistage simultané de N. gonorrhoeae et de C. trachomatis.
- Les délais de rendu des résultats sont plus courts que pour la culture.
- L’automatisation permet l’adaptation aux grandes séries.
Plusieurs trousses commercialisées sont utilisables en France, elles utilisent des principes différents : Polymerase Chain Reaction (PCR), Ligase Chain Reaction (LCR), Strand Displacement Amplification (SDA), Transcription-Mediated Amplification (TMA). La PCR, LCR et SDA amplifient l’ADN bactérien, alors que la TMA amplifie l’ARN ribosomal bactérien. Ces techniques sont développées dans la partie amplification génique du menu « outils diagnostiques«
Pour Neisseria gonorrhoeae, la séquence d’ADN cible est constituée de 201 nucléotides situés dans le gène codant la cytosine-ADN-méthyltransférase. Par précaution, il faut contrôler les résultats positifs par une seconde technique d’amplification utilisant une autre séquence cible.